Auteur : Jordi Ferreiro
Mars 2026
1. Risque de contamination dans les systèmes d’Eau Pharmaceutique
La contamination microbienne et la présence d’endotoxines sont détectées par prélèvement aux Points d’Utilisation (POU) du système. Les pharmacopées applicables définissent des limites microbiologiques admissibles (UFC/mL ou UFC/100 mL, selon le contaminant et le type d’eau).
Par exemple, WFI : dénombrement total < 10 UFC/100 mL.
La vérification et la surveillance systématique de ces paramètres critiques sont principalement réalisées par un échantillonnage représentatif aux points critiques, suivi d’analyses en laboratoire conformément aux critères des pharmacopées et des réglementations.
2. Le concept d’échantillonnage comme garantie de qualité
Un échantillonnage approprié est essentiel pour démontrer la conformité aux exigences microbiologiques du système. Il est complété par des systèmes de mesure en continu, tels que le TOC et la conductivité, qui fournissent des informations supplémentaires sur les performances du système.
Stratégie d’échantillonnage
- Mise en place de points d’échantillonnage périodiques en sortie des équipements critiques
- Définition de plages et de niveaux de fonctionnement appropriés, distincts des plages de conception des instruments
Ces données permettent d’établir une stratégie de contrôle qualité critique pour la qualification et l’exploitation du système :
- Niveaux d’alerte et d’action
- Plages de conception, de fonctionnement normal et acceptable
Un système doit respecter les conditions de conception et fonctionner dans la plage acceptable validée afin d’être conforme aux BPF (GMP).
3. Systèmes de surveillance en continu
Selon l’Annexe 1 des BPF/GMP de l’UE, les systèmes de WFI doivent intégrer une surveillance en continu (TOC et conductivité), qui peut être plus représentative de la performance globale que l’échantillonnage ponctuel.
Limites de l’échantillonnage microbiologique conventionnel
- Délai long pour obtenir les résultats (minimum 72 h)
- Détection limitée aux micro-organismes cultivables
- Sensible aux erreurs humaines lors du comptage des UFC
- Fournit des valeurs estimées et partielles
- Incapacité à détecter les cellules viables non cultivables (VBNC)
- Risque de faux positifs dû à une contamination externe
- Coûts élevés liés aux investigations de déviations et aux arrêts opérationnels
Alternatives de surveillance en continu
Il existe actuellement des systèmes basés sur la détection par fluorescence bactérienne ou la coloration de l’ADN cellulaire, permettant d’estimer en temps réel la charge microbiologique de l’eau, comme solution complémentaire pour réduire les limitations des méthodes conventionnelles.
4. Types de vannes d’échantillonnage recommandés
Toutes les vannes du système doivent être sanitaires, à membrane et sans zones mortes (ZDL : Zero Dead Leg). Cela inclut les vannes des points d’utilisation et les vannes d’échantillonnage, qui doivent également disposer d’un drainage orientable.
Recommandations opérationnelles :
- Ouverture périodique des vannes pour minimiser les risques de contamination
- Ne pas utiliser de vannes à bille ou à siège non sanitaires
- Pour les connexions par flexible, assurer un stockage permettant un drainage complet
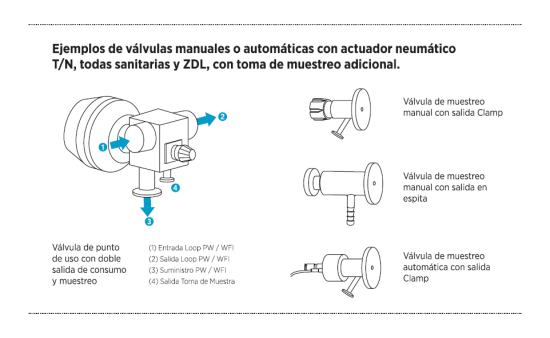
Exemples : vannes manuelles ou automatiques avec actionneur pneumatique T/N, toutes sanitaires et ZDL, avec prise d’échantillonnage supplémentaire.
5. Bonnes pratiques d’échantillonnage pour éviter les faux positifs
L’intégration de vannes d’échantillonnage dans les installations d’Eau Pharmaceutique est un élément clé de conception. Toutefois, il est encore plus critique que les opérations d’échantillonnage soient réalisées de manière rigoureuse et standardisée afin de garantir des échantillons représentatifs et de minimiser les faux positifs microbiologiques.
Une procédure d’échantillonnage (SOP) détaillée et validée permet d’optimiser l’efficacité et de réduire les risques.
Principales recommandations :
Alignement avec les procédures utilisateur
Lors de la phase de conception, il est fortement recommandé de revoir les procédures d’échantillonnage utilisées par l’utilisateur final afin d’ajuster la conception du système et d’identifier des axes d’amélioration.
Emplacement approprié des vannes d’échantillonnage
Les vannes doivent être installées de manière à permettre une ouverture complète et un rinçage préalable. Une accessibilité limitée peut favoriser la contamination externe.
Nettoyage et désinfection avant prélèvement
La procédure doit inclure un nettoyage et une désinfection rigoureux de la vanne avant prélèvement. L’alcool est généralement utilisé, mais la méthode doit être validée avec l’utilisateur. Une désinfection adéquate peut réduire jusqu’à 90 % des excursions microbiologiques.
Purge préalable
Après désinfection, un rinçage d’au moins 30 secondes à débit minimal est requis pour garantir la représentativité de l’échantillon.
Débits recommandés (vitesse > 2,44 m/s) :
- DN 1” : 3 375 L/h
- DN ¾” : 1 710 L/h
- DN ½” : 610 L/h
Surveillance basée sur les tendances
Mettre en place un programme de suivi avec niveaux d’alerte et d’action basés sur l’historique du système.
Inspection et maintenance
Les vannes doivent être inspectées et maintenues régulièrement pour éviter les zones mortes et la formation de biofilm.
6. Recommandations de sanitisation des systèmes d’eau pharmaceutique
Recommandations générales
En complément de l’échantillonnage, une stratégie de sanitisation adaptée est essentielle pour prévenir et traiter les contaminations.
Élimination des composants non sanitaires
Remplacement des composants non conformes suivi d’une sanitisation et d’un suivi renforcé.
Prévention du biofilm
Objectif principal : éviter la formation de biofilm, difficile à éliminer une fois installé.
Types de sanitisation
- Sanitisation thermique (≥ 65 °C)
- Sanitisation à l’ozone (systèmes WFI à froid < 18 °C)
- Sanitisation chimique (moins recommandée)
Sanitisation thermique : température et temps
Méthode la plus robuste, sans ajout de substances.
Recommandée par :
- EudraLex – Annexe 1
- ISPE Baseline Guide (2019)
Temps indicatifs
- 4 h à 65–70 °C
- 2 h à 70–80 °C
- ≥ 1 h à 80–95 °C
Avec rinçages intermittents des vannes.
Continu vs intermittent
La sanitisation continue offre une meilleure protection microbiologique.
La sanitisation intermittente est acceptable si :
- Fréquence élevée
- Adaptée à l’exploitation
- Approche préventive
7. Recommandations de conception
7.1 Sélection des vannes
Définir avec l’utilisateur final selon la SOP.
7.2 Points critiques
Identifier et intégrer les points d’échantillonnage.
7.3 Accessibilité
Garantir un accès adéquat ou prévoir :
- Accès sécurisé
- Gestion des points bas
- Solutions off-line si nécessaire
7.4 Composants
Utiliser uniquement :
- Vannes sanitaires ZDL
- Sorties supplémentaires de prélèvement/purge si nécessaire
