Autor: Jordi Ferreiro. Marzo 2026
1 Riesgo de contaminación en los sistemas de Agua Farmacéutica
La contaminación microbiana y la presencia de endotoxinas se detectan mediante la toma de muestras en los Puntos de Uso (POU) del sistema. Las farmacopeas aplicables establecen límites microbiológicos admisibles (UFC/ml o UFC/100 ml, según contaminante y tipo de agua).
Por ejemplo, WFI: recuento total < 10 UFC/100 ml.
La verificación y monitorización sistemática de estos parámetros críticos se realiza principalmente mediante la toma representativa de muestras en los puntos críticos y su posterior análisis en laboratorio siguiendo los criterios establecidos por farmacopea y regulaciones.
2 Concepto de muestreo como garantía de calidad
El muestreo adecuado es esencial para demostrar el cumplimiento de los requerimientos microbiológicos del sistema. Se complementa con sistemas de instrumentación en continuo, como TOC y conductividad, que proporcionan información adicional sobre el rendimiento del sistema.
Estrategia de muestreo
- Disponer de puntos de muestreo periódicos a la salida de los equipos críticos.
- Definir rangos y niveles de operación adecuados, diferenciándolos de los rangos de diseño de los instrumentos.
Estos datos permiten establecer una estrategia de control de calidad crítica para la cualificación y operación del sistema:
- Niveles de alerta y acción
- Rangos de diseño, operación aceptable y normal
Un sistema debe cumplir las condiciones de diseño y operar dentro del rango aceptable probado para cumplir con GMP.
3 Sistemas de monitorización en continuo
Según Anexo 1 de las BPF/GMP de la UE, los sistemas de WFI deben incorporar monitorización en continuo (TOC y conductividad), que puede ser más representativa del rendimiento global que el muestreo discreto.
Limitaciones del muestreo microbiológico convencional
- Tiempo prolongado para resultados (mínimo 72 h).
- Detección limitada a microorganismos cultivables.
- Susceptible a error humano en recuento de UFC.
- Obtención de valores estimados y parciales.
- Incapacidad para detectar células viables no cultivables (VBNC).
- Riesgo de falsos positivos por contaminación externa.
- Costes elevados asociados a investigación de desviaciones y paradas operativas.
Alternativas de monitorización en continuo
Actualmente existen sistemas basados en la detección por fluorescencia bacteriana o tinción de ADN celular, que permiten estimar en tiempo real la carga microbiológica del agua, como solución complementaria que permita evitar o reducir las limitaciones del sistema convencional.
4 Tipos de válvulas de muestreo recomendables
Todas las válvulas del sistema deben ser sanitarias, de diafragma y sin tramos muertos (ZDL: Zero Dead Leg). Esto incluye válvulas de puntos de uso y válvulas de muestreo, que además deben tener drenaje orientable.
Recomendaciones operativas:
- Apertura periódica de válvulas para minimizar riesgos de contaminación.
- No usar válvulas de bola o asiento no sanitarias.
- En conexiones con manguera, asegurar almacenamiento que permita drenaje completo.
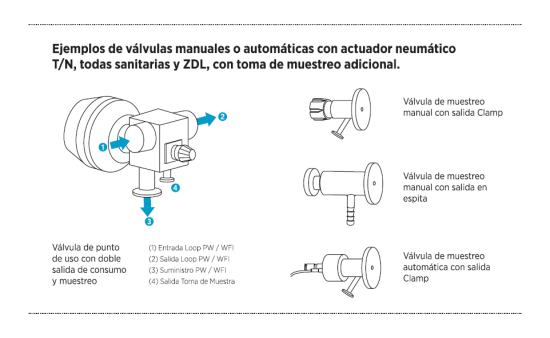
Ejemplos: válvulas manuales o automáticas con actuador neumático T/N, todas sanitarias y ZDL, con toma de muestreo adicional.
5 Pautas y procedimientos de muestreo para evitar falsos positivos.
La incorporación de válvulas de muestreo en las instalaciones de Agua Farmacéutica es un elemento clave de diseño. No obstante, resulta aún más crítico que la operativa de muestreo se realice de forma rigurosa y estandarizada para garantizar muestras representativas y minimizar falsos positivos microbiológicos.
Un Procedimiento de Muestreo (Sampling SOP) detallado y validado permite optimizar la eficiencia y reducir riesgos.
Las pautas principales son:
- Alineación previa con los procedimientos de muestreo del usuario
Durante la fase de diseño resulta altamente recomendable revisar los procedimientos de muestreo utilizados por el usuario final. Esta revisión permite ajustar el diseño del sistema y detectar oportunidades de mejora según tipo de instalación, accesibilidad y nivel de automatización de las válvulas y puntos de uso (POUs).
- Ubicación adecuada de las válvulas de muestreo
Las válvulas de muestreo deben instalarse en posiciones que permitan su apertura completa y enjuague previo. Ubicaciones de difícil acceso pueden favorecer contaminación externa y falsos positivos.
- Limpieza y desinfección previa de la válvula de muestreo
El procedimiento debe establecer un proceso exhaustivo de limpieza y desinfección de la válvula antes de la toma de muestra. Habitualmente se emplea alcohol, aunque el método debe consensuarse con el usuario según sus protocolos y productos de desinfección autorizados. Una desinfección adecuada puede reducir hasta un 90 % las excursiones microbiológicas.
- Purga previa de la toma de muestra
Tras la desinfección de la válvula, debe realizarse una purga o enjuague previo de la toma de muestra durante al menos 30 s a caudal mínimo, asegurando que la muestra sea representativa del agua circulante y no agua estancada en la válvula o contaminación externa.
El caudal mínimo recomendable se establece para una velocidad de salida > 2,44 m/s, que equivale a los caudales siguientes para tamaños habituales en tubería ASME BPE de salida de la válvula de muestreo:
DN 1”: 3.375 l/h, DN ¾”: 1.710 l/h, o DN ½”: 610 l/h
- Monitoreo basado en tendencias y niveles de alerta/acción
El procedimiento debería complementarse con un programa de monitoreo rutinario con niveles de alerta y acción basados en tendencias históricas de cada instalación, para identificar tempranamente excursiones microbiológicas asociadas al muestreo.
- Inspección y mantenimiento periódico
Las válvulas de muestreo deben someterse a inspecciones y mantenimientos periódicos para asegurar que las válvulas no generen tramos muertos, prevenir biofilm y mantener la integridad microbiológica del sistema.
6 Pautas de Sanitización en sistemas de agua farmacéutica
Recomendaciones generales de sanitización
Además del programa de muestreo, es fundamental establecer una estrategia adecuada de sanitización del sistema, orientada tanto a prevenir episodios de contaminación como a actuar eficazmente en caso de detectarse.
Sin profundizar en todos los aspectos técnicos, se presentan a continuación algunas recomendaciones generales aplicables a sistemas de agua farmacéutica:
- Eliminación de componentes no sanitarios
En caso de detectarse válvulas u otros elementos no sanitarios, se recomienda su sustitución, seguida de una sanitización del sistema y un seguimiento reforzado mediante muestreos posteriores.
- Prevención de la formación de biofilm
El objetivo principal de la sanitización es evitar la formación de biofilm. Una vez desarrollado y con cierto espesor, resulta muy difícil de eliminar incluso con desinfectantes potentes, por lo que las estrategias deben tener siempre un enfoque preventivo.
Tipos de sanitización más habituales
Los métodos de sanitización en sistemas de agua farmacéutica pueden clasificarse, en general, por orden de recomendación y eficacia:
- Sanitización térmica (temperaturas ≥ 65 °C).
- Sanitización mediante ozono, utilizada principalmente en sistemas de WFI con generación en frío y almacenamiento a temperaturas inferiores a 18 °C.
- Sanitización química, menos recomendable debido a que suele requerir paradas prolongadas del sistema y procedimientos adicionales de eliminación de residuos.
Sanitización térmica: influencia de temperatura y tiempo
La sanitización térmica se considera el método más robusto, debido a su elevada eficacia microbiológica y a que no introduce sustancias adicionales en el agua, como ocurre con el ozono, que posteriormente debe ser eliminado.
No obstante, el mayor consumo energético asociado a temperaturas elevadas ha favorecido en algunos casos la adopción de sistemas de generación en frío con sanitización mediante ozono.
La eficacia de la sanitización térmica ha sido ampliamente estudiada, demostrando que la combinación de temperatura y tiempo de contacto es determinante para garantizar la eliminación microbiológica.
Las farmacopeas y organismos regulatorios recomiendan generalmente temperaturas de sanitización a partir de 65 °C, como se recoge, por ejemplo, en:
- EudraLex – Annex 1: Manufacture of Sterile Medicinal Products (EMEA)
- ISPE Baseline Guide for Water and Steam Systems (2019)
Recomendaciones orientativas de tiempo de sanitización térmica
En base a los estudios disponibles, pueden considerarse los siguientes tiempos de sanitización orientativos:
- 4 horas entre 65–70 °C
- 2 horas entre 70–80 °C
- 1 hora mínimo entre 80–95 °C
Durante el proceso se recomienda realizar descargas intermitentes (flushing) en las válvulas, para asegurar el contacto del agua caliente con todas las superficies internas del sistema.
Sanitización continua vs. intermitente
La sanitización térmica continua suele ofrecer mayor protección microbiológica que la intermitente, ya que mantiene el sistema en condiciones menos favorables para el desarrollo microbiano. Además, no genera residuos en el agua —a diferencia de la sanitización con ozono, que posteriormente debe eliminarse— y permite operar con temperaturas o concentraciones más moderadas manteniendo el control microbiológico.
No obstante, la sanitización intermitente puede ser adecuada si se cumplen ciertas condiciones:
- Frecuencia elevada, definida según las tendencias microbiológicas del sistema.
- Adaptación al régimen operativo de la planta, permitiendo sanitizaciones nocturnas o en fines de semana.
- Enfoque preventivo, evitando actuar solo en respuesta a episodios de contaminación que implica riesgo muy elevado de biofilm persistente, muy difícil de eliminar.
7 Recomendaciones de diseño para minimizar riesgos de contaminación y facilitar el muestreo
Desde la perspectiva del muestreo y del control microbiológico, es recomendable considerar los siguientes criterios durante el diseño de sistemas de Agua Farmacéutica:
7.1. Selección de válvulas de muestreo y puntos de uso
Definir, conjuntamente con el usuario final, el tipo de válvulas de muestreo y de válvulas de punto de uso incluyendo toma de muestreo, en función del procedimiento de muestreo vigente. En esta fase también pueden identificarse oportunidades de mejora del procedimiento si fuera necesario.
7.2. Identificación de puntos críticos de muestreo
Identificar y consensuar con el usuario los puntos o equipos críticos del sistema, incorporando en ellos los correspondientes puntos de muestreo para garantizar un control microbiológico representativo.
7.3. Accesibilidad de los puntos de muestreo
Si las ubicaciones inicialmente previstas dificultan la correcta aplicación del procedimiento de muestreo, deben acordarse soluciones que garanticen un acceso adecuado. Entre las opciones posibles:
- Garantizar acceso cómodo a localizaciones elevadas no modificables, de manera que sea posible realizar correctamente el muestreo.
- Gestión de puntos bajos del sistema (sifones): cuando la configuración del loop obligue a su existencia, deben incluirse válvulas que permitan el drenaje completo del sistema para evitar estancamientos, y su uso para muestreo.
- Soluciones excepcionales mediante tramos off-line: cuando no sea posible reubicar el punto de muestreo ni garantizar un acceso adecuado, puede considerarse la automatización de la válvula y la incorporación de un tramo de tubería de drenaje aguas abajo (off-line) hasta una zona accesible. Este tramo deberá finalizar en una válvula sanitaria o clamp desmontable que permita realizar el muestreo tras desinfección de la salida. Definiendo caudales y tiempos de purga (flushing) superiores a los habituales para mayor garantía.
7.4. Recomendaciones generales de componentes del sistema
Como criterio general de diseño, se recomienda utilizar exclusivamente:
- Válvulas sanitarias sin tramos muertos (100 % ZDL) tanto en tomas de muestra como en puntos de uso.
- Salidas adicionales de muestreo o purga en válvulas de punto de uso automáticas o en aquellas conectadas permanentemente a tramos posteriores (off-line) que impidan tomar muestra directamente desde la salida principal, salvo decisión expresa del usuario basada en una evaluación de riesgo.
